La profession médicale s’est émue récemment de la publication du décret 2024-968 du 30 octobre 2024, qui n’est en fait que le décret d’application de l’article 73 de la Loi de Finances de la Sécurité Sociale (LFSS) 2024 (adoptée je vous le rappelle en procédure 49-3), qui lui-même modifie l’article L162-19-1 du Code de la Sécurité Sociale, pour décider que :
La prise en charge par l’assurance maladie d’un produit de santé et de ses prestations éventuellement associées peut être subordonnée au renseignement sur l’ordonnance ou sur un formulaire prévu à cet effet par le professionnel de santé d’éléments relatifs aux circonstances et aux indications de la prescription, lorsque ce produit et, le cas échéant, ses prestations associées présentent un intérêt particulier pour la santé publique, un impact financier pour les dépenses d’assurance maladie ou un risque de mésusage.
Lors de la prescription, le recours au formulaire mentionné au premier alinéa, accessible le cas échéant par un téléservice, peut être exigé afin d’attester le respect du même premier alinéa. Ce document est à présenter au pharmacien ou, le cas échéant, à un autre professionnel de santé en vue de la prise en charge ou du remboursement par l’assurance maladie du produit de santé et de ses prestations éventuellement associées. Il peut être dérogé en tant que de besoin, pour la mise en œuvre du présent alinéa, aux dispositions relatives à l’obligation d’homologation de certains formulaires administratifs prévues aux articles 38 et 39 de l’ordonnance n° 2004-637 du 1er juillet 2004 relative à la simplification de la composition et du fonctionnement des commissions administratives et à la réduction de leur nombre.
Ces éléments ainsi que tout autre élément requis sur l’ordonnance sont transmis au service du contrôle médical par le prescripteur, le pharmacien ou, le cas échéant, par un autre professionnel de santé dans des conditions fixées par voie réglementaire.
Ce qui est étrange, c’est que ça correspond exactement au but affiché de l’actuel article 16 du Projet de Loi de Finance de la Sécurité Sociale (PLFSS) 2025 (oui je sais c’est difficile de suivre), rétoqué par la Commission des Affaires Sociales mais néanmoins discuté en séance publique puisqu’il s’agit d’un PLFSS ; quel intérêt y a-t-il à revoter quasiment la même chose un an après (la justification officielle c’est l’extension aux transports et une clarification pour assurer la bonne application au champ de la Liste des Produits et Prestations) ?
Contrairement à ce que j’ai pu lire ici ou là, il ne s’agit pas de restreindre la liberté de prescription (pour ça il y a bien plus efficace, la dispensation sous condition, et la liste des médicaments concernés est déjà très longue et comprend à ce jour 1882 références !), mais beaucoup plus prosaïquement de faire des économies.
Il s’agit en fait de faire respecter le nouveau dada de l’assurance maladie, les ITR ou Indications Thérapeutiques Remboursables. Mais qu’est-ce donc ? Tout simplement le fait que certains médicaments (le Versatis®, l’Havrix®, les antipaludéens, …) même s’ils ont parfois des indications ET des AMM étendues, ne sont en fait remboursables que dans quelques cas précis : les ITR. En cas de prescription en dehors de l’ITR il convient règlementairement de noter NR ou non remboursable après la ligne de la prescription concernée (et non pas hors AMM qui correspond à une prescription pour une indication non reconnue).
Où trouver cette information ? Elle figure dans le dernier paragraphe des monographies du Vidal, au chapitres des information règlementaires.
En cas de non respect de cette obligation, l’assurance maladie peut mettre en œuvre l’article L133-4 du Code de la Sécurité Sociale et se faire rembourser la prescription non règlementaire par le prescripteur ou le pharmacien (qui se doit de vérifier les conditions de prise en charge lui aussi).
Attention, dans la mesure où ce sont des procédures règlementaires (qui dépendent de la loi et des codes) et non pas conventionnelles (qui elles se réfèrent à la convention), tous les médecins, y compris ceux qui exercent hors convention, peuvent être ciblés.
Il y a déjà plusieurs années que des procédures en ce sens sont lancées régulièrement, notamment pour le Versatis® ou les transports, mais l’assurance maladie était gênée par la difficulté de ciblage. Cette disposition est donc tout simplement faite pour repérer facilement les prescriptions non conformes, et dans un premier temps faire en sorte qu’elles ne soient pas remboursables en l’absence de renseignements.
C’est d’ailleurs un des sujets très nettement mis en avant dans l’actuelle convention, dans son article 60, et on y trouve en particulier ces paragraphes :
Augmenter la part de prescriptions médicales dans les ITR et les durées de traitement recommandées par la HAS, en utilisant les outils d’accompagnement à la prescription de l’Assurance maladie pour quelques molécules identifiées ; accompagner prioritairement la conformité de la prescription des AGLP-1
Viser 80% de prescriptions conformes (NR/ou ITR) et l’atteindre sur quelques molécules prioritaires en utilisant les outils d’accompagnement renforcé à la prescription de l’Assurance maladieDéploiement des nouveaux outils pour les professionnel, en démarrant avec le dispositif de prescription renforcée sur les AGLP-1 disponible avant la fin de l’année 2024 sur Amelipro (certificat établissement (sic!) le respect de l’AMM afin d’éviter le mésusage de ces molécules et de garantir leur disponibilité pour les patients diabétiques).
Ce qui permet de constater que la la première cible de l’Assurance Maladie portera sur les Analogues des GLP-1, avec même un calendrier de mise en place avant la fin de l’année 2024 (donc c’est pour demain).
Parce qu’actuellement il n’existe aucun traitement qui soit soumis aux exigences de l’article L162-19-1, même si on a déjà des choses qui y ressemblent, comme l’inscription sur les ordonnances du motif de prescription du dosage de la vitamine D ou de la détermination du groupe sanguin par exemple.
Il n’est donc absolument pas question de devoir indiquer pour chaque traitement son indication précise.
On peut aussi se poser la question des modalités pratiques : le texte prévoit notamment la possibilité de renseignement sur l’ordonnance. Mais à l’heure actuelle ça ne fait pas partie des dérogations légales au secret médical, il faudrait donc pour ça modifier le Code de la Santé Publique (et le Code Pénal). Parce qu’une ordonnance peut parfaitement passer entre les mains de non professionnels de santé, à qui la divulgation d’un diagnostic est évidemment interdite.
Le même écueil s’applique évidemment aux formulaires mentionnés dans le texte, avec en plus l’enquiquinement de devoir aller les chercher, les remplir, et les donner aux patients. Ce qui va encore impacter un peu plus l’exercice en visite à domicile.
Même chose aussi pour les téléservices (même si ça permet d’éviter la violation du secret professionnel) : c’est long et compliqué à faire, et c’est inaccessible en visite.
Il semble toutefois que ce soit la voie privilégiée par l’assurance maladie, qui parle « d’utiliser les outils d’accompagnement renforcé à la prescription », ce qui nous promet encore une belle usine à gaz. Avec probablement comme conséquence une baisse drastique des prescriptions, devant la complexité et la lourdeur de la procédure, et le report sur d’autres molécules. On l’avait bien vu de 2014 à 2018, quand la rosuvastatine et l’ezetimibe nécessitaient une procédure d’entente préalable. Les chiffres de prescription avaient sombré, alors qu’ils sont en très nette progression depuis : il suffit de regarder les graphiques de la ROSP, tous les médecins étaient « dans les clous » de 2016 à 2018, et les chiffres ne cessent de monter depuis pour arriver à quasiment 25% des prescriptions :
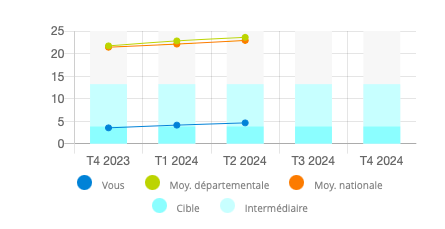
Mais c’est peut-être finalement là le but recherché : compliquer à ce point la vie des prescripteurs qu’ils laissent tomber les molécules « dangereuses ».
En attendant de voir ce que l’avenir nous réserve, je conseille tout de même à tous nos consœurs et confrères de bien regarder leurs prescriptions d’analogues du GLP-1 : ce sera à coup sûr la prochaine cible des contrôles de la CNAM et des procédures de reprises d’indus.
